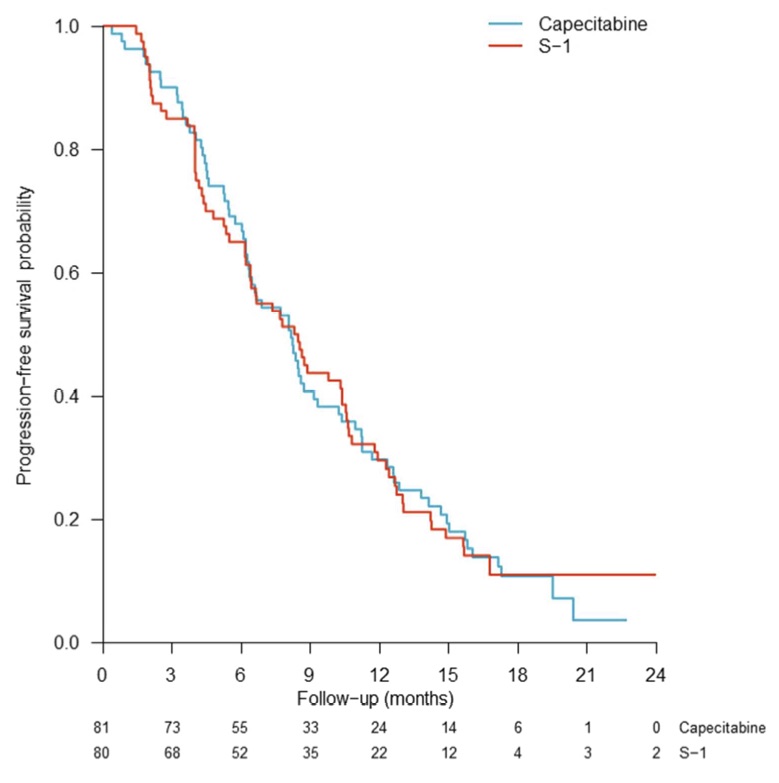
Randomised phase III trial of S-1 versus capecitabine in the first-line treatment of metastatic colorectal cancer: SALTO study by the Dutch Colorectal Cancer Group.
本日は、薬剤部の福田先生の代理で薬学の学生田代さんが抄読会を担当してくれました。呼吸器・内科全般の抄読会ですが、大腸癌の化学療法についてでした。大変勉強になったので、ある程度範囲は決めなくてもいいのかもと、考えさせられた抄読会でした。
<背景>
Capecitabineの主要な副作用として手足症候群(HFS)が有名である。S-1は消化管癌に対して使用される経口フルオロピリミジンであり、Capecitabineとほぼ同様の効果を持ち、アジア人に対してはCapecitabineよりもHFS出現率が低いと報告されている。本研究は転移性直腸がんのある欧米人患者に対し1st
lineとしてCapecitabineとS-1を使用した際のHFS出現率を比較した。
<患者背景、目的>
オランダ27施設研究161人を対象とした
・18歳以上、PS0-2、肝腎・骨髄機能低下がない1st line患者を対象とした。
・除外基準
6か月以内にその他治療を行っている場合
腫瘍縮小後に根治的治療を予定している
過去5年に他の悪性腫瘍に罹患している
Capecitabineに対し抵抗性が示されている
循環器疾患を有している
治療:Capecitabine(70歳以下1250mg/m2、70以上1000mg/m2をday1-14) あるいは
S-1(30mg/m2 day1-14)にて加療、Bevacizumabの併用は許容された。
患者の拒否、PD、毒性が強く継続不可、となるまで3週間おきに継続された。
<評価>
3週間おきにNational Cancer
Institute Common Toxicity Critera(NCI CTC)を使用し毒性を評価、9週間おきにCTにて効果を評価した。更に患者に日記を義務付け、それを元に言及されていない副作用を確認した。
PE:HFS (全grade)
SE:G3 HFS、RDI、PFS、RR、OS
<結果>
全gradeのHFS出現率はcaptcitabineで73%、S-1で45%であった。Grade 3以上はそれぞれ21% 対4%であった。特にG2-3の頻度はcapecitabineで多く、投与2-3か月後での出現が多かった。Bevacizumabとcapecitabineの併用療法ではHFSの出現がやや多かったものの、優位な差とはならなかった。その他のAEとしてはS-1療法では下痢の出現頻度がより多かった。
中央値20.2か月のフォローの後、capecitabine群では90%、S-1群では88%の患者がPDあるいは死亡した。PFSはcapecitabineで8.2か月、S-1で8.4か月であった。Capecitabine/S-1とBevacizumabの併用群でのPFSは8.7か月、単独群では6.6か月であった。12か月/18か月後のOSはcapecitabineで67%/50%、S-1で62%/41%とPFS,OS,RRに関しては優位な差は認めなかった。
<考察>
消化器悪性腫瘍に対して外来化学療法を行う際はXELOX,SOXが主流であるが、XELOXはHFSの出現頻度が多いことが以前から知られていた。HFSの原因物質としては代謝産物であるα-fluoro-β-alanine(FBAL)が知られているが、S-1はcapecitabineと比較して1/18程度のFBAL濃度であり、これが遠因として考えられる。CapecitabineによるHFSがどんな人で出現しやすいかは不明である。
肺がんでもS-1を使用することはあり、稀に手足症候群は出現する。加療方法としては休薬・ある程度濃度が下がるまで対症療法を行うこととなる。
S-1はtegafur、5-chloro-2,4-dihydroxypyridine、potassium oxonateを含んでいる経口のフルオロピリミジンである。
5-FUは代謝経路の中でDNA合成に必要なTSを阻害する部分と、DNA合成とは直接関係しないFBALに返還される経路とがあり、DPDによってFBALへと代謝されてしまう。そこでDPDの阻害剤(5-chloro-2,4-dihydroxypyridine)を加えることで効率的にDNA合成阻害経路へ進めることができる。HFSの原因としてFBALが指摘されており、これがS-1にてHFSが少ない理由と考えられる。
(担当薬剤部田代、まとめ児玉)